2025年6月24日,《临床肿瘤学杂志》(Journal of Clinical Oncology)发表了靶向HER3的抗体偶联药物(ADC)HER3-DXd(patritumab deruxtecan,代号:U3-1402/MK-1022)在既往接受含铂化疗和免疫治疗后进展但无EGFR激活突变的晚期或转移性非小细胞肺癌(NSCLC)患者中的新疗效数据(U31402-A-U102研究)。
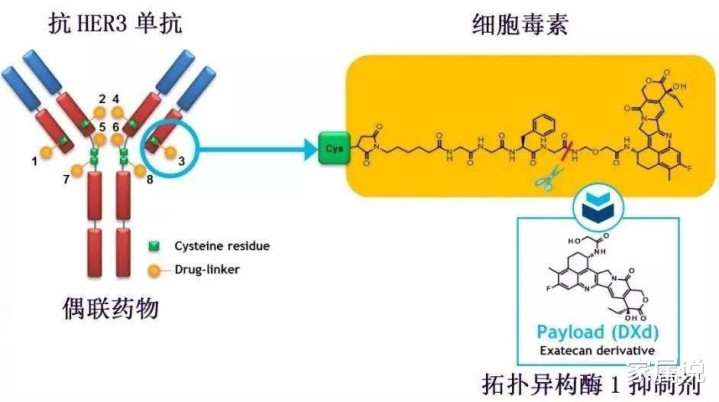
HER3-DXd(通用名:Patritumab deruxtecan,代号:U3-1402)是一款靶向HER3的ADC药物,采用第一三共公司专有的DXd ADC技术设计,由人源化抗HER3抗体与拓扑异构酶I抑制剂有效载荷,通过一个四肽连接子连接而成。
HER3是受体酪氨酸激酶EGFR家族成员,与细胞异常增殖和存活有关。约25%~30%的肺癌具有EGFR激活突变,据估计约83%的NSCLC肿瘤表达HER3蛋白,这可能与转移发生率增加、生存期降低和对标准护理治疗的耐药性有关。
需要注意的是,2025年5月,默克宣布自愿撤回其和第一三共共同开发的HER3-DXd用于治疗既往接受过两种或两种以上全身治疗的局部晚期或转移性EGFR突变NSCLC成年患者的BLA申请,默克称此决定是基于III期临床研究(HERTHENA-Lung02)总生存期(OS)未达到统计学意义的顶线结果。
通用名:Patritumab deruxtecan(HER3-DXd)
代号:U3-1402/MK-1022
靶点:HER3
厂家:Daiichi Sankyo(第一三共公司)
美国首次获批:尚未获批
中国首次获批:尚未获批
临床数据
在U31402-A-U102研究的队列2中,共有47例NSCLC患者接受HER3-DXd 5.6mg/kg治疗,每3周一次。这些患者携带除常见EGFR激活突变外的驱动基因组改变或未确定的驱动基因组改变。所有患者既往均有铂类化疗,95.7%(45/47)患者既往有免疫治疗。19.1%(9/47)的患者接受了先前的靶向治疗,所有患者都患有已确定的驱动基因改变(EGFR Ex20ins,n=4;ALK融合和ROS1融合,各n=2;RET融合,n =1)。
在纳入队列2的总体人群中,经确认的客观缓解率(ORR)为27.7%(n=47),中位反应持续时间(DOR)为8.1个月;疾病控制率(DCR)为74.5%。中位无进展生存期(PFS)为5.5个月,中位OS为15.2 (95% CI, 10.8至17.7)个月。大多数患者(44例中有38例具有基线和基线后目标病变评估)通过BICR评估,目标病变的直径总和有所减少。这表明,在治疗过程中肿瘤的大小有了显著的缩小。
此外,HER3-DXd在有或没有确定的驱动基因组改变的肿瘤患者亚群中的疗效相似,ORR分别为28.6%和26.9%。在已确定的驱动基因组改变的肿瘤患者亚组中观察到持久的反应。5例肿瘤有KRAS或NRAS突变的患者中有3例证实有应答(所有PR)。4例EGFR Ex20ins突变患者均有SD的最佳总缓解(BOR)。在没有确定的驱动基因组改变的肿瘤患者亚组中也观察到持久的反应。
在安全性方面,所有患者均出现≥1次治疗不良事件(TEAE);最常见的是恶心(66.0%)、贫血(51.1%)和食欲减退(51.1%)。≥3级TEAE发生率为72.3% (34/47);最常见的是中性粒细胞减少症(25.5%)、疲劳(17.0%)和血小板减少症(14.9%)。
小结
总之,在这组异质性的既往治疗患者中,HER3-DXd治疗在广泛的肿瘤HER3膜表达水平内显示出具有临床意义的疗效。这种观察到的疗效,以及可耐受的安全性,值得进一步的临床评估。未来将进行更多关于HER3-DXd在有或没有常见EGFR激活突变的NSCLC患者中的研究,无论是单药治疗还是联合用药。
【重要提示】所有文章信息仅供参考,具体治疗谨遵医嘱!
